Некоммерческое акционерное общество
АЛМАТИНСКИЙ УНИВЕРСИТЕТ ЭНЕРГЕТИКИ
И СВЯЗИ
Кафедра физики
МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
Методические указания по выполнению расчетно-графических работ
для студентов специальности 5В071700
– Теплоэнергетика
Алматы, 2014
СОСТАВИТЕЛИ: Мажитова Л.Х., Калшабеков А.С., Наурызбаева Г.К. Молекулярная физика и термодинамика. Методические указания по выполнению расчетно-графических работ для студентов специальности 5В071700-Теплоэнергетика. –Алматы: АУЭС, 2014. – 29с.
Методические указания включают расчетно-графические задания (РГР), методические рекомендации и требования к оформлению и содержанию РГР, список необходимой литературы.
Ил.12 , табл.12 , библиограф. – 12 назв.
Рецензент: канд.тех.наук, доцент АУЭС Туманов М.Е.
Печатается по плану издания некоммерческого акционерного общества «Алматинский университет энергетики и связи» на 2014 год.
Ó НАО «Алматинский университет энергетики и связи», 2014 г.
Введение
Изучение профессионально направленного курса физики в высшем техническом учебном заведений создаёт фундаментальную базу инженерных знаний и умений, практических навыков, формирует основу инженерно – технического мышления, другие профессионально значимые качества будущих инженеров.
Основными целями курса согласно Государственному стандарту образования являются:
1) Формирование представления о современной физической картине мира.
2) Формирование знаний и умений использовать:
- основные понятия, законы и модели механики, электродинамики, колебаний и волн, квантовой физики, статистической физики и термодинамики, зонной теории твёрдого тела;
- методы теоретического и экспериментального исследования физики;
- численные оценки порядков величин, характерных для различных разделов физики.
3) Формирование опыта:
- постановки и решения задач анализа и расчёта характеристик колебаний механических, электромагнитных и комбинированных систем;
- постановки и решения основных задач расчёта электрических и магнитных полей;
- экспериментальной проверки результатов решения указанных задач.
Курс физики изучает физические явления, понятия, законы, модели и теории в их внутренней взаимосвязи. Курс «Молекулярная физика и термодинамика» изучает разделы классической физики «Молекулярно-кинетическая теория идеальных газов», «Основы термодинамики», «Реальные газы. Тепловые машины. Элементы физической кинетики», «Жидкость. Поверхностное натяжение. Уравнение Бернулли. Явление переноса».
Приобретённые знания и умения составляют ту основу, которая необходима при изучении дисциплин «Техническая гидродинамика», «Гидравлика», «Теоретические основы теплотехники», «Теплотехнические измерения» и др.
Весь курс «Молекулярная физика и термодинамика» состоит из четырех кредитов (модулей), по каждому из которых студенты очной формы обучения выполняют расчетно – графическую работу (РГР) по трем уровням сложности (А, В и С), заочной – контрольные работы - по двум уровням (А, В).
В настоящем руководстве приведены варианты расчетно-графических работ, разделенные, по мере возрастания сложности их выполнения, на три уровня усвоения знаний: А, В и С. Критерии разделения задач таковы:
- задания уровня А - это задачи и качественные вопросы, требующие, в основном, умения решать задачи по заданному образцу;
-задания уровня В требуют умений решать типовые задачи по известному алгоритму;
- задания уровня С требуют умений выявлять внутренние связи в конкретной, достаточно сложной, физической ситуации и применять знание общих методов.
Каждый студент самостоятельно выбирает уровень заданий и получает при распределении старостой группы номер варианта. Это распределение должно быть утверждено преподавателем, ведущим практические занятия в группе.
1 Методические рекомендации по выполнению заданий расчетно-графических работ
Решение задач при изучении курса физики в техническом вузе имеет исключительно большое значение для будущих специалистов. Оно учит анализировать изучаемые явления, выделять главные факторы, отвлекаясь от случайных и несущественных деталей, учит моделировать реальные физические и физико-технические процессы. Задачи развивают навык в использовании общих законов материального мира для решения конкретных вопросов, имеющих практическое или познавательное значение.
Невозможно научиться решать задачи по физике, не зная и не понимая теории. Поэтому при выполнении расчетно-графической работы необходима самостоятельная проработка теоретического материала по темам задания и усвоение основных понятий, законов, теорем и принципов.
Процесс решения поставленной физической задачи состоит, как правило, из трех основных этапов. На первом, физическом, этапе проводится анализ условия задачи, выполняется рисунок, схема или векторная диаграмма для ее наглядной интерпретации; затем, на основании тех или иных законов, составляется система уравнений, в число неизвестных которой входят и искомые величины.
На втором, математическом, этапе находят решения системы уравнений, т.е. получают решения задачи сначала в общем виде, а затем, произведя вычисления, числовой ответ задачи.
После того как получено общее решение, необходимо провести его анализ. На этом, третьем, этапе выясняют, как и от каких физических величин зависит найденная величина, в каких условиях эта зависимость проявляется. При анализе числового ответа проверяют размерность полученной величины и оценивают правдоподобность полученного ответа, то есть соответствие числового ответа физически возможным значениям искомой величины.
2 Требования к оформлению и содержанию расчетно-графических (контрольных) работ
Каждую расчетно-графическую (контрольную) работу выполняют в отдельной (школьной) тетради или набирают на компьютере. На обложке или титульном листе указывают дисциплину и номер работы, вариант, кем работа выполнена, кто её проверил, дату сдачи на проверку. Работу выполняют аккуратно, рисунки делают карандашом при помощи линейки.
Образец заполнения титульного листа
РГР №1, М 1 (Контрольная работа №1 – для студентов заочной формы обучения) по дисциплине «Молекулярная физика и термодинамика»
студента группы БРЭ – 10 –5 Ахметова К.М..
(Шифр 255330). Вариант 10.
Условие задачи переписывают полностью, без сокращений. Затем его записывают с помощью общепринятых символических обозначений в краткой форме под заглавием «Дано». Заданные числовые значения переводят в единицы СИ. Решение каждой задачи необходимо сопроводить пояснениями, раскрывающими смысл и значение используемых обозначений, указывающими физические законы и принципы, положенные в основу решения. После того как задача решена в общем виде, т.к. получен ответ в виде расчётной формулы, производят вычисления, руководствуясь при этом правилами приближённых вычислений. Получив численный ответ, следует оценить его правдоподобность; такая оценка позволит в ряде случаев обнаружить ошибочность полученного результата.
В конце работы необходимо указать, каким учебником или учебным пособием студент пользовался при изучении физики.
Если контрольная работа студентами-заочниками пересылается по электронной почте, все требования, касающиеся её оформления, пояснения решений, также должны быть выполнены. В случае, если контрольная работа при рецензировании не была зачтена, студент обязан исправить ошибки и представить работу на повторную рецензию. Повторная контрольная работа представляется вместе с незачтенной. Рецензент может пригласить студента для беседы по существу решения задач.
Сроки сдачи РГР указаны в графике учебного процесса.
2.1 Правила выбора варианта контрольной работы для студентов-заочников
Номер варианта выбирается по двум последним цифрам шифра (номера зачетной книжки) студента следующим образом:
- если предпоследняя цифра шифра нечетная, номера задач берутся из соответствующей таблицы с 1 по 10 варианты, если четная – с 11 по 20 варианты;
- последняя цифра шифра определяет номер варианта.
2.2 Пример решения и оформления задачи
Задача. Какая часть от общего числа молекул азота, находящегося при температуре Т = 300 К и атмосферном давлении обладает скоростями, отличающимися от наиболее вероятной не более, чем на 2,0 м/с?
Дано:
Т=300 К
![]()
![]() .
.
Решение.
При атмосферном давлении
и температуре 300 К азот можно считать идеальным газом. В отсутствие внешних
сил молекулы идеального газа подчиняются закону распределения Максвелла.
Согласно закону Максвелла число молекул ![]() , относительные скорости которых лежат в интервале от и до
и + ∆и при условии, что ∆и « и, равно:
, относительные скорости которых лежат в интервале от и до
и + ∆и при условии, что ∆и « и, равно:
![]() . Относительная
скорость
. Относительная
скорость ![]() в нашем случае равна и=1, поэтому
в нашем случае равна и=1, поэтому
![]() .
.
Вычислим наиболее вероятную скорость vв
vв = ![]() ≈ 422 (м/с);
≈ 422 (м/с);
∆и=![]() .
.
Таким образом, условие ![]() <<u выполняется.
Следовательно:
<<u выполняется.
Следовательно:
![]() .
.
Итак, молекулы азота, обладающие при Т=300 К скоростями, которые лежат в интервале от (vв – 2,0) м/с до (vв + 2,0) м/с, составляют от общего числа долю, равную
∆N/N =0,84%.
3 Расчетно-графическая работа № 1 - «Молекулярно-кинетическая теория идеальных газов»
Цель расчетно-графической работы № 1 - формирование опыта постановки и решения задач, анализа и расчёта характеристик идеального газа.
Таблица 3.1 – Варианты заданий
|
Вариант |
А.Г. Чертов, А.А. Воробьёв «Задачник по физике». -М., 2006. |
В.С.Волькенш-тейн. «Сборник задач по общему курсу физики». -М., 2006. |
Физика. Задания к практическим занятиям (в электронном варианте). |
Приложение А |
|
1 |
9.1; 8.9; 8.5 |
5.41; 5.3 |
8.1 |
1 |
|
2 |
8.2; 9.4; 8.6 |
5.21; 5.46 |
8.5 |
2 |
|
3 |
9.7; 8.3; 8.11 |
5.5; 5.7 |
8.9 |
3 |
|
4 |
8.10; 9.12; 8.14 |
5.14; 5.8 |
8.13 |
4 |
|
5 |
8.13; 9.15; 9.17 |
5.9; 5.29 |
8.3 |
5 |
|
6 |
8.43; 8.31; 8.20 |
5.31; 5.17 |
8.7 |
6 |
|
7 |
8.21; 8.23;8.35 |
5.13; 5.15 |
8.11 |
7 |
|
8 |
8.44; 8.24; 8.28 |
5.6; 5.16 |
8.15 |
8 |
|
9 |
8.29; 8.18; 8.33 |
5.17; 5.19 |
8.17 |
9 |
|
10 |
8.30; 8.32; 8.34 |
5.20; 5.22 |
8.2 |
10 |
|
11 |
8.27; 8.37; 9.14 |
5.2; 5.23 |
8.6 |
11 |
|
12 |
8.36; 8.38; 8.40 |
5.24; 5.4 |
8.10 |
12 |
|
13 |
8.41; 8.16; 8.45 |
5.27; 5.11 |
8.14 |
13 |
|
14 |
8.42; 8.22; 8.1 |
5.30; 5.32 |
8.16 |
14 |
|
15 |
8.1; 9.3; 9.5 |
5.10; 5.33 |
8.4 |
15 |
|
16 |
9.2; 8.4; 9.6 |
5.34; 5.36 |
8.8 |
16 |
|
17 |
8.7; 9.9; 9.11 |
5.35; 5.37 |
8.12 |
17 |
|
18 |
9.8; 9.10; 8.12 |
5.38; 5.40 |
8.19 |
18 |
|
19 |
9.13; 8.15; 8.17 |
5.39; 5.1 |
8.20 |
19 |
|
20 |
8.39; 9.16; 9.18 |
5.47; 5.49 |
8.18 |
20 |
Т а б л и ц а 3.2 – Варианты контрольных заданий для студентов-заочников (нечетные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение А |
|||||
|
0 |
9.1 |
8.27 |
8.38 |
8.37 |
8.33 |
8.34 |
5; 20 |
|
1 |
8.2 |
8.36 |
8.16 |
8.32 |
8.28 |
9.14 |
1; 18 |
|
2 |
9.7 |
8.41 |
8.22 |
8.18 |
8.35 |
8.40 |
7; 14 |
|
3 |
8.10 |
8.42 |
9.3 |
8.24 |
8.20 |
8.45 |
9; 16 |
|
4 |
8.13 |
8.1 |
8.4 |
8.23 |
9.17 |
8.1 |
2; 13 |
|
5 |
8.43 |
9.2 |
9.9 |
8.31 |
8.14 |
9.5 |
3; 12 |
|
6 |
8.21 |
8.7 |
9.10 |
9.15 |
8.11 |
9.6 |
6; 19 |
|
7 |
8.44 |
9.7 |
8.15 |
9.12 |
8.6 |
9.11 |
4; 17 |
|
8 |
8.29 |
9.8 |
9.16 |
8.3 |
8.5 |
8.12 |
9; 11 |
|
9 |
8.30 |
9.13 |
8.39 |
9.4 |
8.9 |
8.17 |
8; 15 |
Т а б л и ц а 3.3 – Варианты контрольных заданий для студентов-заочников (чётные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение А |
|||||
|
0 |
8.21 |
8.38 |
9.9 |
8.33 |
8.34 |
8.27 |
7; 14 |
|
1 |
8.44 |
8.16 |
9.10 |
8.28 |
9.14 |
8.36 |
9; 16 |
|
2 |
8.29 |
8.22 |
8.15 |
8.35 |
8.40 |
8.41 |
2; 13 |
|
3 |
8.30 |
9.3 |
9.16 |
8.20 |
8.45 |
8.42 |
5; 20 |
|
4 |
8.1 |
8.4 |
8.39 |
9.17 |
8.1 |
9.1 |
1; 18 |
|
5 |
9.2 |
8.37 |
8.31 |
8.14 |
9.5 |
8.2 |
9; 11 |
|
6 |
8.7 |
8.32 |
9.15 |
8.11 |
9.6 |
9.7 |
8; 15 |
|
7 |
9.7 |
8.18 |
9.12 |
8.6 |
9.11 |
8.10 |
3; 12 |
|
8 |
9.8 |
8.24 |
8.3 |
8.5 |
8.12 |
8.13 |
6; 19 |
|
9 |
9.13 |
8.23 |
9.4 |
8.9 |
8.17 |
8.43 |
4; 17 |
4 Расчетно-графическая работа № 2 - «Основы термодинамики»
Цель расчетно-графической работы № 2 - формирование опыта постановки и решения задач, анализа и расчёта основ термодинамики
Таблица 4.1 – Варианты заданий
|
Вариант |
А.Г. Чертов, А.А. Воробьёв «Задачник по физике». -М., 2006. |
В.С. Волькенштейн. «Сборник задач по общему курсу физики». -М., 2006. |
Физика. Задания к практическим занятиям (в электронном варианте). |
Приложение Б |
|
1 |
11.1; 11.20; 11.40 |
5.69; 5.88 |
9.1 |
1 |
|
2 |
11.5; 11.25; 11.44 |
5.73; 5.161 |
9.6 |
2 |
|
3 |
11.8; 11.29; 11.48 |
5.78; 5.166 |
9.11 |
3 |
|
4 |
11.12; 11.33; 11.50 |
5.82; 5.171 |
9.16 |
4 |
|
5 |
11.2; 11.21; 11.41 |
5.70; 5.89 |
9.2 |
5 |
|
6 |
11.6; 11.26; 11. 45 |
5.74; 5.162 |
9.7 |
6 |
|
7 |
11.9; 11.30; 11.51 |
5.79; 5.167 |
9.12 |
7 |
|
8 |
11.13; 11.34; 11.49 |
5.83; 5.176 |
9.17 |
8 |
|
9 |
11.16; 11.37; 11.52 |
5.87; 5.174 |
9.19 |
9 |
|
10 |
11.3; 11.22; 11.46; |
5.71; 5.90 |
9.3 |
10 |
|
11 |
11.7; 11.27; 11.53 |
5.75; 5.163 |
9.8 |
11 |
|
12 |
11.10; 11.31; 11.62 |
5.80; 5.168 |
9.13 |
12 |
|
13 |
11.14; 11.35; 11.61 |
5.84; 5.173 |
9.18 |
13 |
|
14 |
11.17; 11.38; 11.60 |
5.81; 5.175 |
9.20 |
14 |
|
15 |
11.4; 11.23; 11.43 |
5.72; 5.159 |
9.4 |
15 |
|
16 |
11.7; 11.28; 11.54 |
5.76; 5.164 |
9.9 |
16 |
|
17 |
11.11; 11.32; 11.59 |
5.85; 5.169 |
9.14 |
17 |
|
18 |
11.15; 11.36; 11.68 |
5.86; 5.170 |
9.15 |
18 |
|
19 |
11.18; 11.39; 11.47 |
5.77; 5.165 |
9.10 |
19 |
|
20 |
11.19; 11.24; 11.44 |
5.73; 5.160 |
9.5 |
20 |
Т а б л и ц а 4.2 – Варианты контрольных заданий для студентов-заочников (нечетные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение А |
|||||
|
0 |
11.1 |
11.19 |
11.20 |
11.24 |
11.40 |
11.44 |
5; 20 |
|
1 |
11.5 |
11.18 |
11.25 |
11.39 |
11.44 |
11.47 |
1; 18 |
|
2 |
11.8 |
11.15 |
11.29 |
11.36 |
11.48 |
11.68 |
7; 14 |
|
3 |
11.12 |
11.11 |
11.33 |
11.32 |
11.50 |
11.59 |
9; 16 |
|
4 |
11.2 |
11.7 |
11.21 |
11.28 |
11.41 |
11.54 |
2; 13 |
|
5 |
11.6 |
11.4 |
11.26 |
11.23 |
11.45 |
11.43 |
3; 12 |
|
6 |
11.9 |
11.17 |
11.30 |
11.38 |
11.51 |
11.60 |
6; 19 |
|
7 |
11.13 |
11.14 |
11.34 |
11.35 |
11.49 |
11.61 |
4; 17 |
|
8 |
11.16 |
11.10 |
11.37 |
11.31 |
11.52 |
11.62 |
9; 11 |
|
9 |
11.3 |
11.7 |
11.22 |
11.27 |
11.46 |
11.53 |
8; 15 |
Т а б л и ц а 4.3 – Варианты контрольных заданий для студентов-заочников (чётные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение А |
|||||
|
0 |
11.6 |
11.40 |
11.24 |
11.23 |
11.4 |
11.26 |
7; 14 |
|
1 |
11.9 |
11.44 |
11.39 |
11.38 |
11.17 |
11.30 |
9; 16 |
|
2 |
11.13 |
11.48 |
11.36 |
11.35 |
11.14 |
11.34 |
2; 13 |
|
3 |
11.16 |
11.50 |
11.32 |
11.31 |
11.10 |
11.37 |
5; 20 |
|
4 |
11.3 |
11.41 |
11.28 |
11.27 |
11.7 |
11.22 |
1; 18 |
|
5 |
11.20 |
11.19 |
11.43 |
11.44 |
11.45 |
11.1 |
9; 11 |
|
6 |
11.25 |
11.18 |
11.60 |
11.47 |
11.51 |
11.5 |
8; 15 |
|
7 |
11.29 |
11.15 |
11.61 |
11.68 |
11.49 |
11.8 |
3; 12 |
|
8 |
11.33 |
11.11 |
11.62 |
11.59 |
11.52 |
11.12 |
6; 19 |
|
9 |
11.21 |
11.7 |
11.53 |
11.54 |
11.46 |
11.2 |
4; 17 |
5 Расчетно-графическая работа № 3 - «Реальные газы. Тепловые машины. Элементы физической кинетики»
Цель расчетно-графической работы №3 - формирование опыта постановки и решения задач, анализа и расчёта реальных газов, тепловых машин и элементов физической кинетики.
Таблица 5.1 – Варианты заданий
|
Вариант |
В.С. Волькенш-тейн «Сборник задач по общему курсу физики». -М., 2006. |
А.Г. Чертов, А.А. Воробьёв «Задачник по физике». -М., 2006. |
Физика. Задания к практическим занятиям (в электронном варианте). |
Приложение В |
|
1 |
5.195, 5.216, 6.1 |
11.53 |
9.31 |
1 |
|
2 |
5.196, 5.217, 6.2 |
11.54 |
9.32 |
2 |
|
3 |
5.197, 5.218, 6.3 |
11.55 |
9.33 |
3 |
|
4 |
5.198, 5.219, 6.4 |
11.56 |
9.34 |
4 |
|
5 |
5.199, 5.220, 6.5 |
11.57 |
9.35 |
5 |
|
6 |
5.200, 5.221, 6.6 |
11.58 |
9.36 |
6 |
|
7 |
5.201, 5.222, 6.7 |
11.59 |
9.37 |
7 |
|
8 |
5.202, 5.223, 6.8 |
11.60 |
9.38 |
8 |
|
9 |
5.203, 5.224, 6.9 |
11.61 |
9.39 |
9 |
|
10 |
5.204, 5.225, 6.10 |
11.62 |
9.40 |
10 |
|
11 |
5.205, 5.226, 6.11 |
11.63 |
9.41 |
11 |
|
12 |
5.206, 5.227, 6.12 |
11.64 |
9.42 |
12 |
|
13 |
5.207, 5.228, 6.13 |
11.65 |
9.43 |
13 |
|
14 |
5.208, 5.229, 6.14 |
11.66 |
9.44 |
14 |
|
15 |
5.209, 5.221, 6.15 |
11.67 |
9.45 |
15 |
|
16 |
5.210, 5.230, 6.16 |
11.71 |
9.46 |
16 |
|
17 |
5.211, 5.223, 6.17 |
11.73 |
9.47 |
17 |
|
18 |
5.212, 5.231, 6.18 |
11.75 |
9.48 |
18 |
|
19 |
5.213, 5.225, 6.19 |
11.72 |
9.49 |
19 |
|
20 |
5.214, 5.227, 6.20 |
11.74 |
9.50 |
20 |
Т а б л и ц а 5.2 – Варианты заданий для студентов-заочников (нечетные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение А |
|||||
|
0 |
11.53 |
11.67 |
11.62 |
11.58 |
11.53 |
11.71 |
5; 20 |
|
1 |
11.54 |
11.71 |
11.71 |
11.59 |
11.54 |
11.73 |
1; 18 |
|
2 |
11.55 |
11.73 |
11.71 |
11.60 |
11.55 |
11.75 |
7; 14 |
|
3 |
11.56 |
11.75 |
11.73 |
11.61 |
11.56 |
11.72 |
9; 16 |
|
4 |
11.57 |
11.72 |
11.75 |
11.62 |
11.64 |
11.74 |
2; 13 |
|
5 |
11.63 |
11.74 |
11.53 |
11.71 |
11.63 |
11.58 |
3; 12 |
|
6 |
11.64 |
11.61 |
11.54 |
11.73 |
11.64 |
11.59 |
6; 19 |
|
7 |
11.65 |
11.62 |
11.55 |
11.75 |
11.65 |
11.60 |
4; 17 |
|
8 |
11.66 |
11.63 |
11.56 |
11.72 |
11.66 |
11.61 |
9; 11 |
|
9 |
11.67 |
11.64 |
11.57 |
11.74 |
11.64 |
11.62 |
8; 15 |
Т а б л и ц а 5.3– Варианты заданий для студентов-заочников (четные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение А |
|||||
|
0 |
11.53 |
11.74 |
11.63 |
11.63 |
11.71 |
11.58 |
7; 14 |
|
1 |
11.54 |
11.61 |
11.64 |
11.64 |
11.73 |
11.59 |
9; 16 |
|
2 |
11.55 |
11.62 |
11.65 |
11.65 |
11.75 |
11.60 |
2; 13 |
|
3 |
11.56 |
11.63 |
11.66 |
11.66 |
11.72 |
11.61 |
5; 20 |
|
4 |
11.57 |
11.64 |
11.67 |
11.64 |
11.74 |
11.62 |
1; 18 |
|
5 |
11.71 |
11.58 |
11.53 |
11.53 |
11.67 |
11.62 |
9; 11 |
|
6 |
11.73 |
11.59 |
11.54 |
11.54 |
11.71 |
11.71 |
8; 15 |
|
7 |
11.75 |
11.60 |
11.55 |
11.55 |
11.73 |
11.71 |
3; 12 |
|
8 |
11.72 |
11.61 |
11.56 |
11.56 |
11.75 |
11.73 |
6; 19 |
|
9 |
11.74 |
11.62 |
11.64 |
11.57 |
11.72 |
11.75 |
4; 17 |
6 Расчетно-графическая работа № 4 - «Жидкость. Поверхностное натяжение. Уравнение Бернулли. Явление переноса»
Цель расчетно-графической работы №4 - формирование опыта постановки и решения задач, анализа и расчёта свойств и динамики жидкости.
Таблица 6.1 – Варианты заданий
|
Вариант |
А.Г. Чертов, А.А. Воробьёв «Задачник по физике». -М., 2006 |
В.С.Волькенштейн «Сборник задач по общему курсу физики». -М., 2006. |
Физика. Задания к практическим занятиям (в электронном варианте) |
Приложение Г |
|
1 |
34.1; 34.6; 34.30 |
18.1; 18.21 |
23.1 |
1 |
|
2 |
34.11; 34.16; 34.3 |
18.6; 18.16 |
23.6 |
2 |
|
3 |
34.21; 34.22; 34.24 |
18.11; 18.3 |
23.11 |
3 |
|
4 |
34.26; 34.9; 34.29 |
18.16; 18.4 |
23.16 |
4 |
|
5 |
34.2; 34.7; 34.10 |
18.2; 18.22 |
23.2 |
5 |
|
6 |
34.12; 34.17; 34. 15 |
18.7; 18.1 |
23.7 |
6 |
|
7 |
34.22; 34.1; 34.29 |
18.12; 18.5 |
23.12 |
7 |
|
8 |
34.27; 34.14; 34.20 |
18.17; 18.9 |
23.17 |
8 |
|
9 |
34.30; 34.5; 34.17 |
18.19; 18.7 |
23.20 |
9 |
|
10 |
34.3; 34.8; 34.2 |
18.3; 18.6 |
23.3 |
10 |
|
11 |
34.13; 34.18; 34.27 |
18.8; 18.2 |
23.8 |
11 |
|
12 |
34.23; 34.16; 34.26 |
18.13; 18.21 |
23.13 |
12 |
|
13 |
34.28; 34.4; 34.8 |
18.18; 18.20 |
23.18 |
13 |
|
14 |
34.29; 34.24;34.6 |
18.15; 18.1 |
23.19 |
14 |
|
15 |
34.4; 34.9; 34.17 |
18.4; 18.5 |
23.4 |
15 |
|
16 |
34.14; 34.19; 34.8 |
18.9; 18.19 |
23.9 |
16 |
|
17 |
34.24; 34.12; 34.15 |
18.20; 18.2 |
23.14 |
17 |
|
18 |
34.25; 34.13; 34.3 |
18.21; 18.3 |
23.15 |
18 |
|
19 |
34.15; 34.20; 34.1 |
18.10; 18.18 |
23.10 |
19 |
|
20 |
34.5; 34.10; 34.11 |
18.5; 18.2 |
23.5 |
20 |
Т а б л и ц а 6.2 – Варианты контрольных заданий для студентов-заочников (нечетные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение Г |
|||||
|
0 |
34.1 |
34.5 |
34.10 |
34.6 |
34.40 |
34.11 |
5; 20 |
|
1 |
34.11 |
34.15 |
34.20 |
34.16 |
34.3 |
34.1 |
1; 18 |
|
2 |
34.21 |
34.25 |
34.13 |
34.22 |
34.24 |
34.3 |
7; 14 |
|
3 |
34.26 |
34.24 |
34.12 |
34.9 |
34.29 |
34.15 |
9; 16 |
|
4 |
34.2 |
34.14 |
34.19 |
34.7 |
34.15 |
34.8 |
2; 13 |
|
5 |
34.12 |
34.4 |
34.9 |
34.17 |
34.29 |
34.17 |
3; 12 |
|
6 |
34.22 |
34.29 |
34.24 |
34.1 |
34.15 |
34.6 |
6; 19 |
|
7 |
34.27 |
34.28 |
34.4 |
34.14 |
34.29 |
34.8 |
4; 17 |
|
8 |
34.30 |
34.23 |
34.16 |
34.5 |
34.20 |
34.26 |
9; 11 |
|
9 |
34.3 |
34.13 |
34.18 |
34.8 |
34.17 |
34.27 |
8; 15 |
Т а б л и ц а 6.3 – Варианты контрольных заданий для студентов-заочников (чётные)
|
Вариант |
Номера задач (Чертов А.Г., Воробьёв А.А. «Задачник по физике».-М., 2006.) |
Приложение Г |
|||||
|
0 |
34.17 |
34.29 |
34.9 |
34.4 |
34.17 |
34.11 |
7; 14 |
|
1 |
34.6 |
34.15 |
34.24 |
34.29 |
34.1 |
34.1 |
9; 16 |
|
2 |
34.8 |
34.29 |
34.4 |
34.28 |
34.14 |
34.3 |
2; 13 |
|
3 |
34.26 |
34.20 |
34.16 |
34.23 |
34.5 |
34.15 |
5; 20 |
|
4 |
34.27 |
34.17 |
34.18 |
34.13 |
34.8 |
34.8 |
1; 18 |
|
5 |
34.12 |
34.40 |
34.6 |
34.10 |
34.5 |
34.1 |
9; 11 |
|
6 |
34.22 |
34.3 |
34.16 |
34.20 |
34.15 |
34.11 |
8; 15 |
|
7 |
34.27 |
34.24 |
34.22 |
34.13 |
34.25 |
34.21 |
3; 12 |
|
8 |
34.30 |
34.29 |
34.9 |
34.12 |
34.24 |
34.26 |
6; 19 |
|
9 |
34.3 |
34.15 |
34.7 |
34.19 |
34.14 |
34.2 |
4; 17 |
Приложение А
А.1 Газ сначала расширился изотермически, затем был сжат адиабатно. Работы расширения и сжатия равны по модулю. Сравнить объём газа в начале и в конце процесса.
А.2 В газе происходят процессы: а) изохорное нагревание; б) адиабатное сжатие. Начальные температуры равны. Количество теплоты, поглощаемое в случае а, равняется работе над газом в случае б. Сравнить конечные температуры.
А.3 Сравнить работы, производимые газом в циклах I и IІ (см. рисунок А.1):
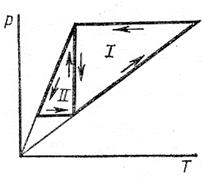
Рисунок А.1
А.4 Известна зависимость n(r) концентрации молекул газа от координат.
Найти распределение вероятностей dω(r) координат молекул. Объём газа V.
А.5 Газ из состояния 1 переходит в состояние 2 в одном случае непосредственно по изобаре, а в другом - сначала по изохоре 1-3, затем - по изобаре 3-4 и, наконец, по изохоре 4-2. Доказать прямым расчетом, что приращение энтропии в обоих случаях одинаково (см. рисунок А.2).
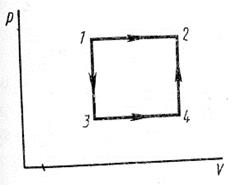
Рисунок А.2
А.6 Как зависит от давления средняя скорость молекул идеального одноатомного газа при адиабатическом сжатии или расширении?
А.7 Тепловая машина работает по циклу, состоящему из двух изохор и двух изобар. Доказать, что при работе машины энтропия системы «нагреватель - газ – холодильник» увеличивается. Как при этом изменяется энтропия газа? Теплоёмкости нагревателя и холодильника считать безграничными.
А.8 Равновесный идеальный газ находится во внешнем поле, в котором
потенциальная энергия его молекулы равна u(r), температура газа Т. Концентрация молекул газа в точке с радиус-вектором r0 равна n0. Определить концентрацию молекул в точке с радиус-вектором r.
А.9 Энтропия процесса линейно растет с температурой. Как должна зависеть от температуры теплоемкость этого процесса (см. рисунок А.3)?
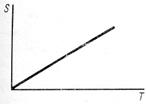
Рисунок А.3
А.10 Получить дифференциальное уравнение для зависимости давления р идеального газа с температурой Т, находящегося в однородном поле тяжести, от высоты h; для чего рассмотреть цилиндр бесконечно малой высоты dh. Решить это уравнение в предположении, что температура газа не зависит от h и р(h=0)=p0. В тех же предположениях найти зависимость от высоты концентрации молекул n.
А.11 Два тела с начальными температурами Т1 и Т2 (причем Т1>Т2) приведены в соприкосновение. От окружающей среды тела изолированы, массы и теплоёмкости тел одинаковы. Как изменяется суммарная энтропия этих тел в процессе выравнивания температуры?
А.12 При каком значении температуры число молекул, скорости которых лежат в фиксированном интервале (u, u+du), максимально?
А.13 Определить наименьшее возможное давление идеального газа в процессе, происходящем по закону T=T0+αV2, где T0 и α - положительные постоянные, V – объем моля газа. Изобразить примерный график этого процесса в параметрах р , V.
А.14 Определите, насколько возрастает температура у подножия водопада высотой h=50 м?
А.15 В цилиндре, закрытом поршнем, находится газ (см. рисунок А.4). Сверху поршень прижат пружиной, упругие свойства которой подчиняются закону Гука. Нарисовать в координатах рV изменение состояния газа при нагревании и определить совершаемую при этом работу, если объём газа изменяется от V1 до V2 и давление - от р1 до р2.
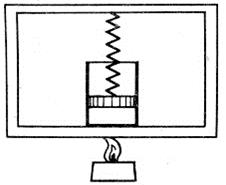
Рисунок А.4
А.16 Максвелловское распределение может быть представлено не только как функция скоростей, но и как функция энергий молекул. Эта функция определяет число молекул, энергия которых лежит в интервале от w до w+dw: dN=N0f(w)dw.
Требуется найти выражение этой функции и определить, относится ли она только к определённому газу или пригодна для любого газа.
А.17 По оси абсцисс (см. рисунок А.5) отложено количество теплоты, подведенное к идеальному газу, а по оси ординат - совершенная газом работа. Одна из прямых на рисунке - изотерма, две другие - изобары для двух газов. Начальные состояния ( давление, температура, объём) обоих газов одинаковы. Масштабы по обеим осям одинаковы. Какая прямая какому процессу соответствуют? Сколько степеней свободы у каждого газа? (Колебательные степени свободы не учитывать). Графики каких процессов совпадают с координатными осями?
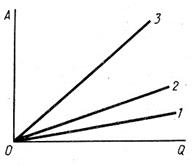
Рисунок А.5
А.18 Вследствие хаотичности движения молекул длины свободного пробега молекул имеют разнообразное значение. Если по оси ординат откладывать логарифмы числа молекул (см. рисунок А.6), длина свободного пробега которых больше некоторого расстояния х, а по оси абсцисс - расстояние х, то соответствующая зависимость изображается прямой линией с отрицательным наклоном согласно уравнению lg N=lgN0-ax. Как на основании этого графика определить длину свободного пробега молекул?
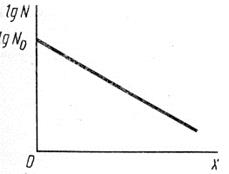
Рисунок А.6
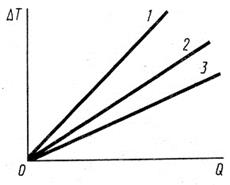
А.19 Прямые (см. рисунок А.7) изображают зависимость изменения температуры от количества подведенной теплоты для различных процессов изменения состояния одноатомного и двухатомного газов. Каким процессам соответствуют эти прямые? Графики каких процессов совпадают с координатными осями? Начальные состояния (температура, объём, давление) обоих газов одинаковы.
Рисунок А.7
А.20 Газ из молекул массы массы m находится в равновесном состоянии с температурой Т. Написать выражение для распределения вероятностей dw(vx)=φ(vx)dvx для компоненты vx скорости молекул газа. Нарисовать на одном чертеже графики зависимости φ(vx) для: а) v=v1, T=T1; б) m=4m1, T=T1; в) m=m1, T=4T1; г) m=αm1, T=αT1, где α - некоторое число. Чему равны площади под кривыми?
Приложение Б
Б.1 В тонкостенном сосуде объема V, стенки которого поддерживаются при постоянной температуре, находится идеальный газ. Сосуд помещен в вакуум. Как будет меняться с течением времени концентрация n молекул газа внутри сосуда, если в его стенке сделать очень малое отверстие площади S? Определить время t1/2, по истечении которого давление газа внутри сосуда уменьшится в 2 раза. Считать, что истечение газа происходит настолько медленно, что оно практически не нарушает равновесность состояния во всем сосуде, за исключением малой области вблизи отверстия. Температуру газа в сосуде считать постоянной и равной внешней температуре.
Б.2 Распределение Максвелла для компоненты скорости
(например vx) имеет вид dw (vx)=φ(vx)dvx=A exp[-mv2x
/(2kT)]dvx. Воспользовавшись значением интеграла Пуассона
∫ ехр(-αξ2)dξ=![]() π/α,
отнормировать распределение Максвелла. Что происходит с максимальным значением
φ при: а) увеличение температуры Т; б) увеличении массы m?
Вычислить <V2x>.
π/α,
отнормировать распределение Максвелла. Что происходит с максимальным значением
φ при: а) увеличение температуры Т; б) увеличении массы m?
Вычислить <V2x>.
Б.3 Известно отношение γ=Ср/Сv для некоторого идеального газа. Получить уравнение адиабаты (d'Q=0) этого газа в переменных V,T; p,V; p,T. Почему отношение γ называют показателем адиабаты идеального газа?
Б.4 На рисунке Б.1 показана зависимость φ(vx). Какой физический смысл имеют заштрихованные площади?
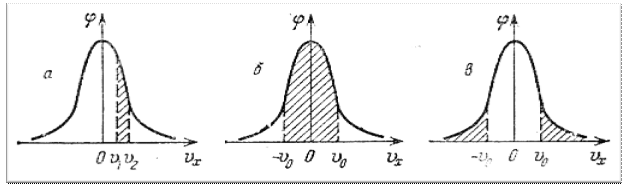
Рисунок Б.1
Б.5 Откачанный тонкостенный сосуд, стенки которого поддерживаются при постоянной температуре, погружен в атмосферу идеального газа с постоянной концентрацией n0, поддерживаемого при той же температуре. Как будет меняться с течением времени концентрация молекул газа внутри сосуда, если в его стенке сделать очень малое отверстие?
Б.6 Все ординаты кривой 2 в два раза больше, чем соответствующие координаты кривой 1. Чем отличаются функции распределения молекул по скоростям, изображаемые этими кривыми (см. рисунок Б.2)?
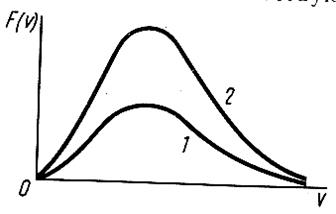
Рисунок Б.2
Б.7 На рисунке Б.3 представлены адиабаты двух газов - гелия и углекислого газа. Какая кривая какому газу принадлежит?
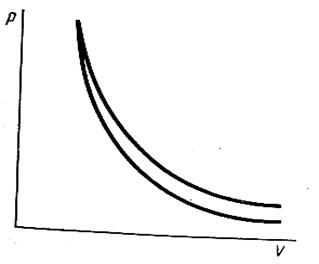
Рисунок Б.3
Б.8 Какая из прямых на рисунке Б.4 правильно изображает в логарифмическом масштабе зависимость средней квадратичной скорости молекул от температуры?
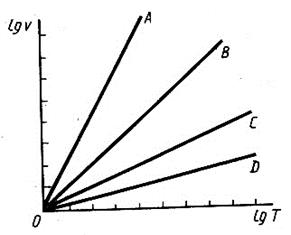
Рисунок Б.4
Б.9 Зависит ли давление идеального газа: а) от концентрации молекул; б) от температуры; в) от массы молекулы?
Б.10 В сосуде постоянного объема производится нагревание один раз m граммов некоторого газа, другой раз 2m граммов этого же газа. Вычертить кривые зависимости давления от температуры для этих двух случаев. Указать различие в расположении кривых.
Б.11 Газ находится в тепловом равновесии. Отличны ли от нуля: а) <v x>; б) <v>; в) <v>?
Б.12 В теплоизолированном сосуде, разделённом на две секции подвижным и теплопроницаемым поршнем, содержатся два разных газа. Одинаковы ли в обеих секциях в состоянии равновесия: а) средние энергии молекул; б) плотности молекул; в) средние квадратические скорости молекул? Трением при перемещении поршня пренебречь.
Б.13 В равновесном процессе в газе, представленном графиком АВС (см. рисунок Б.5), точки А и С лежат на адиабате. Отличны ли от нуля, в этом процессе: а) количество поглощенной газом теплоты; б) изменение энтропии?
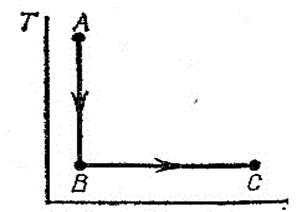
Рисунок Б.5
Б.14 Какое повышение температуры идеального газа: а) изобарическое; б) изохорическое, требует большего количества теплоты?
Б.15 Средняя скорость молекул равновесного газа в системе отсчета, где газ как целое покоится, равна <v>. Определите среднюю скорость <vотн> движения молекул газа относительно друг друга.
Б.16 Зная число Авогадро ![]() , плотность вещества
, плотность вещества ![]() и молярную массу М, получите формулы, определяющие
число молекул в произвольной массе вещества.
и молярную массу М, получите формулы, определяющие
число молекул в произвольной массе вещества.
Б.17 Как изменяется средняя арифметическая скорость
теплового движения молекул идеального газа при увеличении давления в процессе,
для которого p~![]() ?
?
Б.18 Изменяется ли давление газа, если: а) молекулы газа диссоциируют при постоянной температуре? б) изменяется температура при постоянной концентрации молекул? Ответы обоснуйте.
Б.19 Согласно МКТ давление газа p~n<>. В каком изопроцессе одновременно с возрастанием n увеличивается и средняя энергия поступательного движения молекулы <Е>? Объясните ответ.
Б.20 Может ли в каком-либо изопроцессе одновременно с возрастанием n уменьшаться средняя энергия поступательного движения молекулы <Е>? Объясните ответ.
Приложение В
В.1 Известны градиент температуры ![]() и теплопроводность
и теплопроводность ![]() . Напишите выражение для плотности потока теплоты
. Напишите выражение для плотности потока теплоты ![]() . Объясните его и укажите единицы
. Объясните его и укажите единицы ![]() в СИ.
в СИ.
В.2 Сосуд, содержащий некоторое количество
одноатомного газа, движется со скоростью ![]() , затем внезапно останавливается. На сколько
увеличится при этом квадрат средней квадратичной скорости молекул? Что такое
средняя квадратичная скорость?
, затем внезапно останавливается. На сколько
увеличится при этом квадрат средней квадратичной скорости молекул? Что такое
средняя квадратичная скорость?
В.3 Принимая молекулу за шарик диаметром определите, какая часть объема, занимаемая газом при нормальных условиях, приходится на его молекулы.
В.4 Объясните, почему снять плотно закрытую крышку сосуда бывает проще после прогрева ее под струей горячей воды.
В.5 Каково содержание одного из основных законов классической статистической физики о равнораспределении энергии по степеням свободы? Как определяется число степеней свободы молекулы?
В.6 Верны ли и почему
приведенные соотношения для смеси двух химически нереагирующих идеальных газов:
![]()
В.7 Верна ли и почему формула приращения внутренней
энергии идеального газа ![]() для процессов: а) изохорного; б) изобарного?
для процессов: а) изохорного; б) изобарного?
В.8 Газ сначала расширился изотермически, затем был сжат адиабатно. Работы расширения и сжатия равны по модулю. Сравните объем газа в начале и конце процесса. Изобразите графики процессов на p-V – диаграмме.
В.9 В чем сходство и различие понятий работа A и теплота Q? Cформулируйте первое начало термодинамики.
В.10 Выведите формулу, выражающую связь между
молярными теплоемкостями ![]() для идеального газа. Поясните физический смысл
универсальной постоянной газа R.
для идеального газа. Поясните физический смысл
универсальной постоянной газа R.
В.11 Докажите, что показатель адиабаты ![]() всегда больше единицы? Почему адиабатный процесс
относится к изопроцессам?
всегда больше единицы? Почему адиабатный процесс
относится к изопроцессам?
В.12 Цикл Карно. Постройте его диаграмму в координатах PV, TS. Зависит ли к.п.д. цикла Карно: а) от положения изотерм; б) от положения адиабат; в) от вида рабочего вещества?
В.13 Первое начало термодинамики иногда несколько вольно формулируют следующим образом: «Невозможно точно восстановить разрушенное». Объясните, как согласовать эти вольные формулировки со строгими формулировками первого и второго начал термодинамики?
В.14 Газ расширяется изотермически от объема ![]() до объема
до объема ![]() при: а) T=
при: а) T=![]() ; б) T=
; б) T=![]() (
(![]() >
>![]() ). Сравните приращения энтропии в этих условиях,
объясните ответ.
). Сравните приращения энтропии в этих условиях,
объясните ответ.
В.15 На основе анализа цикла тепловой машины покажите, какую роль играет холодильник и почему без него невозможен отличный от нуля КПД?
В.16 Начертите и объясните графики зависимости плотности идеального газа в зависимости от температуры при изотермическом, изобарном и изохорном процессах.
В.17 Если газ быстро сжать (например, переместив поршень), то его температура повысится. Когда газ под поршнем расширяется, происходит его охлаждение. Объясните эти изменения температуры с точки зрения молекулярно-кинетической теории, обратив внимание на то, что происходит в тот момент, когда молекулы сталкиваются с движущимся поршнем.
В.18 Не должны ли все предметы, находящиеся при
одинаковой температуре, создавать у нас одинаковые ощущение тепла или холода?
Вы без малейшего колебания надеваете на себя одежду, имеющую комнатную
температуру, примерно ![]() , но попробуйте сесть раздетым в сухую ванную, которая
казалось бы, должна иметь ту же температуру, и вы почувствуете, как велика тут
разница. Почему?
, но попробуйте сесть раздетым в сухую ванную, которая
казалось бы, должна иметь ту же температуру, и вы почувствуете, как велика тут
разница. Почему?
В.19 Преобразуйте функцию распределения Максвелла,
перейдя от переменной ![]() , где – наиболее вероятная скорость молекул. Что дает
такое изменение?
, где – наиболее вероятная скорость молекул. Что дает
такое изменение?
В.20 Как изменяется динамическая вязкость газа ![]() при увеличении объема в процессах: а) изобарном; б)
изотермическом?
при увеличении объема в процессах: а) изобарном; б)
изотермическом?
Приложение Г
Г.1 Как и почему изменяются при изотермическом расширении газа: а) средняя кинетическая энергия молекул; б) средняя длина свободного пробега молекул?
Г.2 Газ находится в закрытом сосуде. Зависят ли и почему от средней скорости теплового движения молекул газа: а) среднее число столкновений молекулы за 1с с другими молекулами; б) средняя длина свободного пробега молекул?
Г.3 Объясните, как изменяется средняя длина свободного
пробега молекул газа: а) при изобарном нагревании; б) при изотермическом
увеличении давления? Изменением эффективного сечения молекул пренебречь.
Постройте графики зависимости средней длины свободного пробега молекул от
температуры ![]() .
.
Г.4 Объясните, как изменяются при изохорном нагревании
газа: а) среднее время между соударениями молекул; б) средняя длина свободного
пробега молекул. Изменением эффективного сечения молекул пренебречь. Постройте
графики зависимости средней длины свободного пробега молекул температуры ![]() и среднего времени между соударениями от температуры.
и среднего времени между соударениями от температуры.
Г.5 Приведите и поясните основное уравнение молекулярно-кинетической теории идеального газа. Почему давление газа зависит от средней энергии поступательного движения молекулы, а не от ее полной энергии?
Г.6 Сформулируйте второе начало термодинамики. В реальных условиях невозможно избежать ни самопроизвольных расширений, ни трения, ни теплового рассеяния. Каков же общий признак у этих процессов? Объясните.
Г.7 Приведите примеры естественных (происходящих самопроизвольно) процессов, в которых порядок сменяется беспорядком. Почему это происходит? Обсудите возможности наблюдения обратных процессов.
Г.8 Имеются два разных газа в цилиндрах, имеющих одинаковые параметры состояния. Один газ одноатомный, другой двухатомный. Сначала они в одинаковой степени расширяются изотермически, а затем адиабатически. Какой из них совершил большую работу при изотермическом расширении? Почему? Какой – при адиабатическом расширении? Почему? Покажите процессы на p,V – диаграмме.
Г.9 Газ переходит из одного и того же начального состояния 1 в одно и то же конечное состояние 2 в результате следующих процессов: а) изотермического; б) изобарного и изохорного. Рассмотрев эти процессы графически, покажите: 1) в каком случае работа расширения максимальна; 2) когда газу сообщается максимальное количество теплоты.
Г.10 Одно из толкований энтропии – мера беспорядка. Что служит основанием этого, почему? Приведите примеры.
Г.11 В газе происходят процессы: а) изохорное нагревание; б) адиабатное сжатие. Начальные температуры равны. Количество теплоты, поглощаемое в случае а, равняется работе над газом в случае б. Сравните конечные температуры.
Г.12 Используя T-S –
диаграмму, докажите, что термический КПД необратимого цикла всегда меньше
коэффициента полезного действия обратимого цикла Карно при тех же значениях ![]() .
.
Г.13 Газ расширяется обратимо: а) изотермически; б) изобарно; в) адиабатно. Начальные и конечные объемы во всех процессах совпадают. В каких случаях прирост энтропии газа минимален и максимален?
Г.14 Изобразите графически изотермический и адиабатный процессы на диаграммах P-V и T-S, проанализируйте эти зависимости. Объясните, почему диаграмму P-V называют рабочей, а диаграмму T-S – тепловой?
Г.15 Теплоемкость является функцией процесса. Как это следует понимать? Почему мы часто используем теплоемкости изохорного и изобарного процессов и никогда – адиабатного и изотермического?
Г.16 Исходя из распределений Максвелла и Больцмана, объясните, почему на Луне нет атмосферы, а скорость рассеяния атмосферы Земли ничтожно мала?
Г.17 Сосуд разделе пористой перегородкой на две равные
части. После того как из обеих частей выкачали воздух, одну из них заполнили
водородом (1), а другую – азотом (2). Начальные давления ![]() обоих газов одинаковы. Нарисуйте схематически график
изменения давления в каждой части сосуда с течением времени.
обоих газов одинаковы. Нарисуйте схематически график
изменения давления в каждой части сосуда с течением времени.
Г.18 Сформулируйте основные положения МКТ явлений переноса. Чем обусловлена общность молекулярно-кинетического механизма явлений переноса различной физической природы?
Г.19 При каких условиях устанавливается максвелловское распределение молекул по скоростям? Охарактеризуйте функцию этого распределения, приведите график f(v) и объясните, почему она асимметрична.
Г.20 Почему явления переноса, называют «тройной аналогией»? Запишите общее уравнение переноса, объединяющее законы Фика, Фурье, Ньютона и объясните смысл входящих в него величин и само уравнение.
Список литературы
1.Трофимова Т.И. Курс физики. – М.: Высшая школа, 2004.
2.Савельев И.В. Курс общей физики: Кн.2: Молекулярная физика и термодинамика. -М.: «Издательство АСТ», 2004.
3.Волькенштейн В.С. Сборник задач по общему курсу физики. -М.: Наука, 2006.
4. Чертов А.Г., Воробьёв А.А.«Задачник по физике». -М.: Изд-во Физико-математич.лит-ры, 2006.
5. Физика 1. Конспект лекций (для студентов очной формы обучения специальностей 050718 – Электроэнергетика, 050717 - Теплоэнергетика). –Алматы: АИЭС, 2006.
6. Дмитриева Е.И. Физика в примерах и задачах. –М.: «Форум, Инфра-М», 2011.
7. Трофимова Т.И. Физика. –М.: «Академия», 2012.
8. Трофимова Т.И. Курс физики с примерами решение задач. Т.1. –М.: «Кнорус», 2010.
Содержание
|
Введение |
3 |
|
1 Методические рекомендации по выполнению заданий расчетно-графических работ |
4 |
|
2 Требования к оформлению и содержанию расчетно-графических (контрольных) работ |
4 |
|
2.1 Правила выбора варианта контрольной работы для студентов-заочников |
5 |
|
2.2 Пример решения и оформления задачи |
5 |
|
3 Расчетно-графическая работа № 1 - «Молекулярно-кинетическая теория идеальных газов» |
7 |
|
4 Расчетно-графическая работа № 2 - «Основы термодинамики» |
9 |
|
5 Расчетно-графическая работа № 3 - «Реальные газы. Тепловые машины. Элементы физической кинетики» |
11 |
|
6 Расчетно-графическая работа № 4 - «Жидкость. Поверхностное натяжение. Уравнение Бернулли. Явление переноса» |
13 |
|
Приложение А |
15 |
|
Приложение Б |
19 |
|
Приложение В |
23 |
|
Приложение Г |
25 |
|
Список литературы |
27 |
Св.план 2014 г., поз.130
Ляйля Хамитовна Мажитова
Калшабеков Арайбек Салыбекович
Гульнара Кадырбековна Наурызбаева
МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
Методические указания по выполнению расчетно-графических работ
для студентов специальности 5В071700
– Теплоэнергетика
Редактор
З.Т. Абдраимова
Специалист по стандартизации Н.К. Молдабекова
Подписано
к печати
Формат
60´84 1/16
Тираж
40 экз.
Бумага
типографская № 1
Объем
1,8 уч. изд.л.
Заказ
___ цена 900 тенге.
Копировально-множительное бюро
Некоммерческое акционерное общество
Алматинский университет энергетики и связи
050013, г. Алматы, Байтурсынова, 126